Dr. Stefaan Van Gool MD PhD is als vooraanstaand expert in tumorimmunologie en neuro-oncologie in kinderen en volwassenen werkzaam als medisch directeur van de Praxis für Immunonkologie & Translationale Medizin in het Duitse Immuno-onkologisch centrum in Keulen. Mede gesteund door Nobelprijswinnaar Professor Steinman heeft Dr. Stefaan Van Gool het baanbrekend onderzoek naar dendritische cellen in tumortherapie opgezet, waardoor hij een van de eerste was in Europa die een patiënt met een glioblastoom behandeld heeft met dendritische cel immuuntherapie. Zijn carrière concentreert zich op één principe: geïndividualiseerde multimodale immuuntherapie.
Geïndividualiseerde Multimodale Immuuntherapie in een therapeutisch strategisch plan
Na een diagnose van een solide of hersentumor is de eerste stap de standaardbehandeling. Deze bestaat uit chirurgie, radiotherapie en/of chemotherapie om de tumor zoveel mogelijk te verwijderen. Echter, wanneer er tumorcellen onbehandeld achterblijven, heeft de kanker de kans om terug te komen. Nieuw ontwikkelde therapieën schakelen daarom het eigen immuunsysteem in om achtergebleven tumorcellen op te ruimen. Het toepassen van het eigen immuunsysteem wordt “geïndividualiseerde immuuntherapie” genoemd. Aangezien immuuntherapie bestaat uit verschillende technieken wordt de combinatie daarvan “multimodale immuuntherapie” genoemd. Geïndividualiseerde multimodale immuuntherapie wordt afgekort naar IMI. Immuuntherapie wordt vermoeilijkt door drie verschillende factoren:
- Het immuunsysteem is getraind om de eigen cellen niet aan te vallen: dit is precies waaruit een tumor bestaat.
- De tumor kan zich verbergen voor het immuunsysteem, en het zelfs actief verzwakken.
- Radio- en chemotherapie verzwakken naast de tumor ook het immuunsysteem.
Het is daarom belangrijk om verschillende behandelingen in meerdere fasen toe te passen: eerst wordt de tumor zelf verzwakt, daarna wordt het immuunsysteem heropgebouwd, en vervolgens wordt het immuunsysteem getraind en ingezet tegen de zich verder ontwikkelende tumor. Voor elke patiënt moet dus een globaal therapeutisch strategisch plan opgebouwd worden.
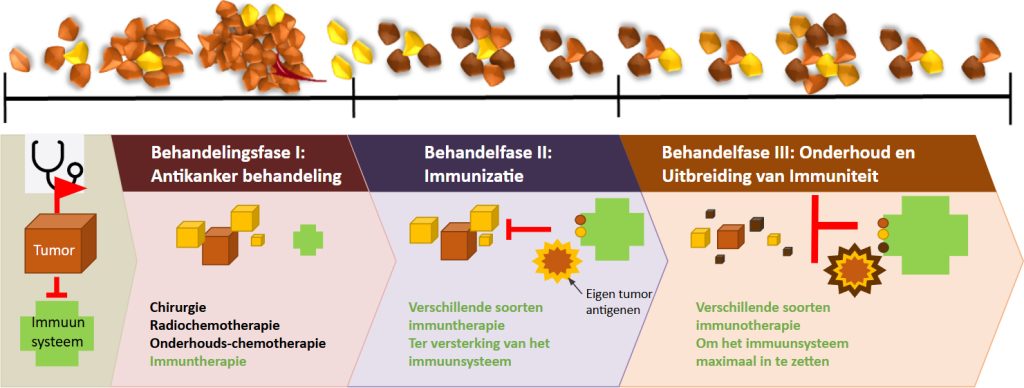
De verschillende fasen
Tijdens de eerste fase van de antikankertherapie wordt de tumor aangepakt met standaardbehandeling. Radio- en chemotherapie verzwakt de tumor, maar ook het immuunsysteem. Hier kunnen al immuuntherapeutische technieken ingezet worden om tumorcellen te doden en het tumor micromilieu te veranderen. De patiënt ondergaat gemoduleerde elektro-hyperthermie: elektromagnetische golven worden door de tumor gezonden. Omdat tumorcellen actiever zijn dan gezonde cellen zijn ze gevoeliger voor hittestress, en worden ze selectief uitgeroeid. Ook krijgt de patiënt injecties met het zogenaamde Newcastle Disease Virus. Dit virus infecteert normaliter alleen vogels, maar kan ook tumorcellen binnendringen doordat deze hun natuurlijke bescherming tegen het virus verloren zijn. Het virus maakt de tumor van binnenuit kapot, en biedt een extra herkenningspunt voor het immuunsysteem om aan te vallen. Tijdens de tweede fase wordt actief een anti-kanker immuunantwoord opgebouwd met vaccinaties. Dit wordt gedaan met behulp van dendritische cellen: hoogst belangrijke cellen van het immuunsysteem die alle andere immuuncellen kunnen activeren, en zo een immuunreactie teweeg kunnen brengen. Deze patiënt-eigen dendritische cellen kunnen in een laboratorium worden geselecteerd en worden getraind met eigen tumorcellen en tumorstoffen, genaamd antigenen, waardoor ze de tumor als bedreiging leren herkennen. Wanneer de dendritische cellen dan weer in het lichaam worden geïntroduceerd, activeren ze het immuunsysteem. Omdat tumorcellen zich kunnen verbergen voor immuuncellen worden checkpoint inhibitors ingezet: deze kunnen bepaalde herkenningspunten van de tumor of immuuncellen afdekken, waardoor de immuuncellen hun werk kunnen doen. Omdat de tumor zich blijft ontwikkelen om zo de aanvallen te kunnen ontsnappen, wordt tijdens de derde fase het immuunsysteem verder versterkt, zodat de tumor herhaaldelijk wordt aangevallen op steeds nieuwe manieren.
Het effect
Geïndividualiseerde multimodale immuuntherapie wordt compleet per patiënt ontworpen: er wordt rekening gehouden met de karakteristieken van de specifieke tumor, welke mutaties deze heeft, wat voor behandelingen de patiënt al ondergaat en de status van het immuunsysteem. Per patiënt wordt afgemeten welke verschillende behandelingen op welk moment het meest behulpzaam zijn. Dit betekent dat er geen extra toxiciteiten ontstaan door deze vormen van immuuntherapie: enkel de eigen immuuncellen en de eigen tumorcellen worden gebruikt om het immuunsysteem te trainen en te versterken.
Dr. Stefaan Van Gool: “Wanneer we naar patiëntengroepen kijken, zien we onder bijvoorbeeld hersentumorpatiënten (specifiek glioblastoom patiënten) een duidelijke verlenging van de gemiddelde levensverwachting bij inzet van IMI. Waar onder de standaardtherapie een gemiddelde levensduur van minder dan twee jaar wordt verwacht, zien we bijna een verdubbeling wanneer patiënten bijkomend IMI ondergaan. Dit is ongezien wanneer therapieën separaat worden gebruikt, of zelfs wanneer verschillende therapieën gecombineerd maar tegelijkertijd worden ingezet, en bevestigt hoe belangrijk het is om verschillende therapieën op verschillende momenten in te zetten.
Naast gemiddelde levensverwachting is natuurlijk ook de kwaliteit van leven van hoog belang om de waarde van een behandeling in te schatten. Daarom wordt elke patiënt herhaaldelijk gevraagd bepaalde gestandaardiseerde vragenlijsten in te vullen, waarmee de patiënt zelf de kwaliteit van leven kan aangeven. Met behulp van deze zelfevaluaties weten we dat niet alleen de levenskwaliteit van veel patiënten stabiel blijft tijdens IMI, maar dat voor sommigen deze zelfs verbetert, ongeacht hoe lang een patiënt onder behandeling is of welk specifiek behandelplan gevolgd wordt. Zelfs wanneer een terugkeer van een tumor zich voordoet, vaak geassocieerd met een sterke daling van kwaliteit van leven, houdt de IMI de levenskwaliteit op peil.
Daarmee kunnen we wetenschappelijk vaststellen dat elke dag gewonnen met behulp van IMI ook echt geleefd kan worden.”
IMI deel van standaardzorg?
Op dit moment zijn veel immuuntherapieën, waaronder ook IMI, enkel toegankelijk als private zorg of als deel van een klinische studie: ze maken geen deel uit van de standaardtherapie. Behandelingen die onder de standaardzorg vallen zijn toegankelijk voor patiënten omdat ze direct door oncologen worden aangeraden, en omdat kosten door verzekeraars vergoed worden. Dit betekent dat immuuntherapieën niet vroegtijdig ingezet worden, en soms door financiële overwegingen of simpelweg onbekendheid buiten bereik blijven van de patiënten die ze het hardst nodig hebben. Dit zou opgelost kunnen worden wanneer IMI geïncludeerd zou worden onder standaardzorg. Wat staat hier in de weg?
Nieuwe therapieën worden enkel gerekend tot de standaardzorg wanneer ze op basis van afdoende bewijs als veilig en effectief bestempeld kunnen worden. Voor het verzamelen van bewijs is een gecompliceerd en duur systeem ontstaan: gerandomiseerde klinische studies. Klinische studies bestaan uit meerdere fasen: tijdens fase 1 wordt de veiligheid van een therapie getest, tijdens fase 2 wordt het nut van een therapie bewezen. Fase 1 en 2 worden vaak gecombineerd uitgevoerd op een kleine groep welingelichte patiënten. Tijdens fase 3 wordt een therapie getest op een zeer grote groep mensen, bestaande uit zowel patiënten als gezonde mensen, die blind een placebo of de therapie krijgen. Dit is vaak een fase die meerdere jaren spant en hoog in kosten oploopt. Er zitten veel voordelen aan het testen van nieuwe therapieën op deze manier, maar ook een aantal grote nadelen. Zo moeten patiënten aan strikte eisen voldoen wat betreft leeftijd, gezondheidsniveau, andere vormen van behandeling, en tumor karakteristieken, om aan een studie deel te mogen nemen. Doordat het enorm veel tijd kost zo’n studie op te zetten, kunnen veel patiënten al geen gebruik meer maken van de behandeling. In sommige landen mogen patiënten alleen meedoen aan een klinische studie wanneer ze zijn uitbehandeld: een groot probleem wanneer de te kort schietende standaardbehandeling langer duurt dat de gemiddelde levensverwachting. Naarmate we meer leren over hoe tumoren in elkaar zitten en hoe ze van elkaar verschillen door persoonsgebonden factoren, winnen gepersonaliseerde en geïndividualiseerde therapieën het aan belangrijkheid. Echter, deze patiënt-specifieke behandelingen kunnen niet getest worden binnen het vereiste gestandaardiseerde protocol in een klinische studie. We moeten ons misschien ook afvragen: zijn vaste klinische studie protocollen de juiste manier om hoog-dynamische ongecontroleerde tumoren te bestrijden? Ten slotte is het vanwege de kosten aantrekkelijker voor bedrijven om standaard therapieën te bekostigen, omdat bij een kant-en-klaar product een makkelijk verdienmodel ontstaat. Gepersonaliseerde en zeker geïndividualiseerde therapieën moeten per persoon ontworpen en gemaakt worden, waardoor de kosten voor elke therapie hoog kunnen oplopen; zeker wanneer een duur voortraject terugverdiend moet worden. Veel therapieën, ondanks hun veiligheid en werkzaamheid, komen niet door deze derde fase van klinische studies heen: slechts 3,4% van de antikankertherapieën die getest worden in klinische studies haalt het tot de patiënt.
Ondanks deze restricties worden klinische studies als noodzakelijk geacht om een nieuwe therapie als veilig en effectief op te nemen binnen de standaardzorg. Aangezien de wetenschap sneller beweegt dan de bureaucratie betekent dit dat er een zeer grote kloof is ontstaan tussen wat mogelijk is en wat mag. Wat betreft de zorg voor glioblastoom-patiënten, bijvoorbeeld, is de standaardzorg al 20 jaar onveranderd gebleven, ondanks dat deze niet voor iedereen aanslaat, en ondanks de vooruitgang in de wetenschap. In bepaalde landen, zoals Duitsland, is het mogelijk voor patiënten om te kiezen voor zorg die nog niet binnen de standaardzorg valt. Dit heet het “Individueller Heilversuch”. Een patiënt wordt compleet geïnformeerd over een mogelijke behandeling en kan zelf de keuze maken deze wel of niet te ondergaan. Hierdoor zijn in Duitsland andere, meer geavanceerde, kankertherapieën wel beschikbaar.
Wanneer patiënten onder het “Individueller Heilversuch” behandeld worden, zijn er veel minder restricties dan bij klinische studies. Er wordt data verzameld van deze patiënten, zogenoemde “Real World Data”, wat vaak een realistischer beeld geeft dan de geselecteerde populatie binnen een klinische studie. Wanneer “Real World Data” als bewijs gebruikt kan worden om therapieën op te nemen binnen de standaardzorg zal er een nieuwe wereld kunnen openen aan opties voor kankerpatiënten. Helaas heeft dit nog een lange weg te gaan.
Dr. Stefaan Van Gools streven
Dr. Stefaan Van Gool staat onder zijn patiënten en medewerkers bekend als een zeer kundige, zeer zorgzame dokter. Patiënten komen van over de hele wereld naar Dr. Stefaan Van Gool voor zijn ongeëvenaarde expertise in geïndividualiseerde kankerzorg. Naast het behandelen en begeleiden van patiënten zet Dr. Stefaan Van Gool zich in om het bewijs dat IMI werkt, gebaseerd op “Real World Data” van zijn eigen praktijk, voor patiënten met vaste en hersentumoren de wereld in te krijgen. Ook werken hij en zijn team aan de bureaucratische acceptatie van “Real World Data” als bewijs, zodat nieuwe behandelmethoden toegankelijk worden voor alle patiënten wereldwijd.